
Una manera de entender cómo funciona un proceso celular es perturbando la actividad de un componente clave del sistema y observando como se ve afectado el proceso. La mayoría de las herramientas para conseguir esta “perturbación” se basan en enfoques genéticos que interfieren en la acción de una proteína o se basan en la administración local de compuestos. Sin embargo, ninguno de estos enfoques es adecuado para investigar eventos transitorios o irreversibles, como en el caso de la endocitosis, porque es difícil o imposible controlar la dinámica de proteínas, la ubicación espacial y el tiempo de la actividad. Estas limitaciones también pueden afectar la eficacia y especificidad de los medicamentos utilizados en la farmacoterapia.
 Ahora, el grupo del CIBER-BBN y el IBEC “Nanoprobes and nanoswitches”, liderado por el Profesor de Investigación ICREA Pau Gorostiza, en colaboración con el IQAC-CSIC, IPMC, IRB, IDIBELL, UB y UAB, publican en la revista Chemical Science un estudio donde desarrollan las primeras pequeñas moléculas inhibidoras de la endocitosis controladas por luz: los dynazos. Estas moléculas, llamadas dynazos, son capaces de inhibir la dinamina, una proteína clave en endocitosis, en condiciones de “no luz”. Al contrario, aplicando la luz visible, los dynazos son inactivados como inhibidores de dinamina y la endocitosis puede tener lugar. La endocitosis es un mecanismo utilizado por todas las células eucariotas para internalizar material extracelular, y regula procesos fisiológicos clave como la captación de nutrientes y de factores de crecimiento. Además, también es la vía de entrada de una variedad de patógenos. El uso de dynazos permitirá controlar con precisión la ubicación espacial y la dinámica de este proceso celular estratégico.
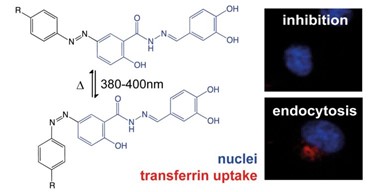
Ahora, el grupo del CIBER-BBN y el IBEC “Nanoprobes and nanoswitches”, liderado por el Profesor de Investigación ICREA Pau Gorostiza, en colaboración con el IQAC-CSIC, IPMC, IRB, IDIBELL, UB y UAB, publican en la revista Chemical Science un estudio donde desarrollan las primeras pequeñas moléculas inhibidoras de la endocitosis controladas por luz: los dynazos. Estas moléculas, llamadas dynazos, son capaces de inhibir la dinamina, una proteína clave en endocitosis, en condiciones de “no luz”. Al contrario, aplicando la luz visible, los dynazos son inactivados como inhibidores de dinamina y la endocitosis puede tener lugar. La endocitosis es un mecanismo utilizado por todas las células eucariotas para internalizar material extracelular, y regula procesos fisiológicos clave como la captación de nutrientes y de factores de crecimiento. Además, también es la vía de entrada de una variedad de patógenos. El uso de dynazos permitirá controlar con precisión la ubicación espacial y la dinámica de este proceso celular estratégico.
Los investigadores han utilizado un diseño racional y escalonado para obtener la primera pequeña molécula regulada por la luz capaz de inhibir la endocitosis a través del control de la dinamina. “Hemos combinado las propiedades farmacológicas del dynasore, un inhibidor de la dinamina, con las propiedades fotocrómicas de un grupo de azobenceno, una de las moléculas sensibles a la luz (fotoswitcherable) más estudiadas”, explica Nuria Camarero, primera coautora del estudio.
Los investigadores caracterizaron en detalle las propiedades fotocromáticas de los dynazos bajo diferentes espectros de luz y espectroscopia de absorción transitoria, y han obtenido moléculas que responden a la luz visible violeta, lo que minimiza los efectos negativos potenciales del uso de la luz UV en sistemas vivos. Además, la actividad biológica de los dynazos, a concentraciones micromolares, fue confirmada por microscopia de fluorescencia confocal, citometría de flujo y microscopia de reflexión interna total (TIRFM) utilizando diferentes líneas celulares.
La herramienta recientemente desarrollada, que permite activar y desactivar de forma remota y reversible la actividad biológica de la dinamina, será sin duda muy relevante para descifrar el papel de la endocitosis en procesos celulares como el crecimiento celular, la diferenciación, la motilidad y la modulación de la señalización de los receptores transmembrana y la transmisión sináptica, entre otros. Los procesos endocíticos también pueden ser dianas para evitar la entrada de patógenos y prevenir infecciones, o matar intencionadamente células por la captación de compuestos tóxicos. “La tecnología de dynazos abre las puertas a la utilización de la luz como activador externo para controlar la actividad farmacológica de compuestos que afecten la endocitosis con una resolución espacio-temporal” concluye el jefe de grupo Pau Gorostiza.
Artículo de referencia:
Núria Camarero, Ana Trapero, Ariadna Pérez-Jiménez, Eric Macia, Alexandre Gomila-Juaneda, Andrés Martín-Quirós, Laura Nevola, Artur Llobet, Amadeu Llebaria, Jordi Hernando, Ernest Giralt, and Pau Gorostiza. Photoswitchable dynasore analogs to control endocytosis with light. Chem. Sci., 2020.
Este estudio se ha realizado en colaboración con: Institute for Advanced Chemistry of Catalonia (IQAC-CSIC), Institut de Pharmacologie Moléculaire et Cellulaire (IPMC), Institute for Research in Biomedicine (IRB Barcelona), Bellvitge Biomedical Research Institute (IDIBELL), Departament de Química, Universitat Autònoma de Barcelona (UAB), Universitat de Barcelona (UB) y el CIBER-BBN.