Investigadores españoles han desarrollado un sofisticado dispositivo microfluídico capaz de reproducir in vitro y en 3 dimensiones la complejidad de diferentes tipos tumorales. Dicho dispositivo permite que las células tumorales crezcan en un entorno 3D dónde los nutrientes y el oxígeno son suministrados de forma controlada a través de unos pequeños capilares, imitando así a los propios vasos sanguíneos del organismo.
Gracias a esta nueva tecnología, es ahora posible reproducir de manera controlada todos los procesos del entorno tumoral, lo que podría ayudar a desarrollar nuevos tratamientos y combinaciones de fármacos que sean más efectivos para el tratamiento de estos tumores.
En este estudio, publicado en Scientific Reports, han participado investigadores del Grupo de Mecánica Aplicada y Bioingeniería (AMB) de la Universidad de Zaragoza, en colaboración con el Grupo de Neuroingeniería Biomédica de la Universidad Miguel Hernández (NBIO), ambos pertenecientes al Centro de Investigación Biomédica en Red de Bioingeniería, Biomateriales y Nanomedicina (CIBER-BBN), junto con el grupo de Inmunidad y Cáncer del Instituto de Investigación Sanitaria Aragón, el Instituto de Tecnología Química de Valencia (ITQ-CSIC) y un equipo de la Universidad de Huddersfield (Reino Unido).
Los tumores son sistemas muy complejos, y su evolución depende no solo de las células tumorales sino también del entorno tridimensional que las rodea y de su interacción con otros tipos celulares. A menudo la proliferación incontrolada de las células tumorales genera una severa falta de nutrientes y oxígeno en el microentorno del tumor. Por lo tanto, las células tumorales se ven obligadas a crecer en un ambiente muy particular y diferente al del resto del organismo, lo que les obliga a adaptarse y desarrollar mecanismos de resistencia frente a esta situación que pueden afectar de forma muy importante a los fármacos que empleamos para su tratamiento. En este contexto, la mayor parte de las investigaciones contra estos tumores se realizan en placas bidimensionales, que no permiten reproducir el entorno real de estos tumores dentro del cuerpo humano. Esto podría explicar por qué muchos tratamientos experimentales, que aparentemente muestran un gran potencial contra estos tumores durante la fase experimental en laboratorio, luego no son capaces de conseguir los mismos resultados en modelos animales reales o en pacientes.
Esta nueva plataforma de cultivos 3D permite observar directamente cómo el metabolismo tumoral lleva al agotamiento progresivo de los nutrientes y el oxígeno, generando la aparición de distintas zonas dentro del tumor. En este entorno hostil, las células tumorales adaptan su velocidad de proliferación en función de la cantidad de alimento de la que disponen para poder sobrevivir.
La reproducción controlada de todos los procesos del entorno tumoral que posibilita esta nueva tecnología podría ayudar a desarrollar nuevos tratamientos y combinaciones de fármacos que sean más efectivos para el tratamiento de estos tumores. Sin embargo, aunque los resultados preliminares son muy prometedores, todos los investigadores implicados advierten que todavía queda mucho trabajo por hacer.
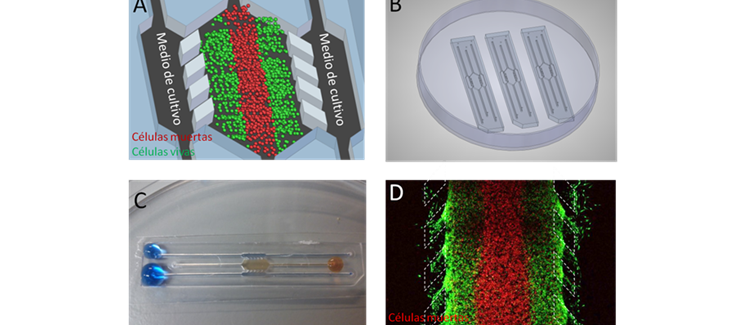
(*) Imagen: A) Esquema del dispositivo microfluídico. Las células tumorales son alojadas en la cámara central en combinación con una matriz proteica tridimensional. Posteriormente, se perfunde medio de cultivo por los canales laterales para proveer de oxígeno y nutrientes al sistema. B) Se pueden construir matrices con varios dispositivos pegados a una placa de Petri. C) Fotografía de un dispositivo en el que se han perfundido líquidos de distintos colores por los laterales y la cámara central. Escala 1 cm. D) Imagen de microscopía confocal del dispositvo. Tras 6 días en cultivo, las células de tumor cerebral (U-251 MG) se tiñeron con colorantes específicos para evaluar su viabilidad. Las células vivas aparecen en verde, mientras que las muertas aparecen en rojo. Los pilares que delimitan la frontera entre la cámara central y los canales laterales se han dibujado en línea blanca discontinua. Escala 400 µm.
Artículo de referencia:
Development and characterization of a microfluidic model of the tumour microenvironment.Jose M. Ayuso, María Virumbrales-Muñoz, Alodia Lacueva, Pilar M. Lanuza, Elisa Checa-Chavarria, Pablo Botella, Eduardo Fernández, Manuel Doblare, Simon J. Allison, Roger M. Phillips, Julián Pardo, Luis J. Fernandez e Ignacio Ochoa. Scientific Reports. 10.1038/srep36086